臨床研究的四個階段:





第一階段 主要招募少量健康志願者,透過觀察臨床表徵和檢查,追蹤實驗性藥物或治 療方法於人體之吸收、分佈、代謝與排泄過程,旨評估其安全性,確定其安全劑量範 圍及副作用。這些研究要在醫院進行。
第二階段 小規模招募患病志願者為對象,一般使用對照組設計,將實驗性藥物或治療 方法以不同劑量形式與現有的治療或安慰劑進行比較,並進一步確定其有效性及安全 性。這些研究可以在研究中心進行。
第三階段 擴大招募數百至數千病人為對象,隨機將病人分配到試驗組或對照組,並 進行雙盲試驗(即醫護人員與病人不會知道組別分配)。與現有的黃金治療方法作比較, 進一步測試其有效性及監測副作用,以確認實驗性藥物或治療方法是否優於或不差於 現有的治療方案。此階段亦是實驗性藥物或治療方法正式在市面上推出的最後階段。 進行時研究團隊一般已掌握到藥物的安全性。這些研究可以在研究中心進行。
第四階段 在藥物正式獲得批准使用後進行大規模安全性追蹤的研究,旨評估有關治 療的長遠效益。
香港臨床研究中心進行的多為第二以及第三階段研究。臨床藥物研究志願參加者在研究中可以發揮積極的作用,獲得使用嶄新研究治療的機會,同時可以通過促進醫學研究以促使新的藥物或治療方案儘 早落地於社區,為病人的福祉作出貢獻。
参加臨床研究對個人及社會的重要性
- 1
最新治療方式:可接觸到最新的治療方式,這些治療方式可能比現有的治療方式更有效,更安全,或者更方便。
- 2
專業及更緊密的醫療照護:不用自費的情況下,可得到專業的醫療照護,研究人員 (包括醫生及護士) 會密切監測您的健康狀況,並提供必要的治療及護理。
- 3
相應的資助:大部份的臨床研究會提供一定的資助,例如交通費等。
- 4
對自己和社會做出貢獻:參加臨床研究可以幫助研究人員更好地了解疾病,從而改善治療方式,及造福更多患者。
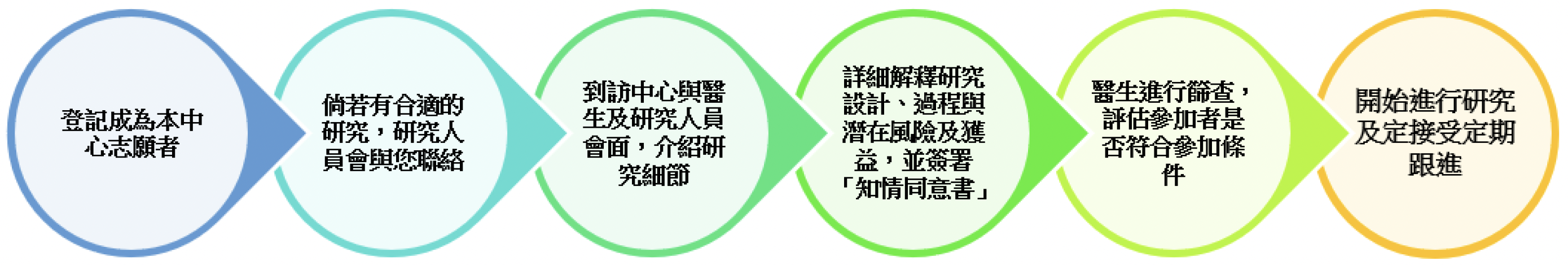
參加臨床研究流程:
FAQ
研究人員如何確保參加者的安全性?
什麼人可以參加臨床藥物研究?
一旦參與了研究後,我有權退出嗎?
在參加臨床藥物研究前有什麼需要考慮?
點擊下面的連結或掃描二維碼,立即註冊成為臨床研究志願者!
個人資料保密文案 局限於在同意書上提及的機構 (例: 本中心,贊助商,與研究有關的機構)有限權取得您的個人資料,確保個人資料保密及受到保障。